《天津卷》高考理综试合试题+参考答案










试读已结束,还剩4页未读,您可下载完整版后进行离线阅读
《《天津卷》高考理综试合试题+参考答案》是由用户上传到老师板报网,类型是数学试卷,大小为1.43 MB,总共有14页,格式为doc。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。更多关于请在老师板报网直接搜索
- 上一篇: 《江西卷》高考文科数学试题+参考答案
- 下一篇: (理全国Ⅰ-Ⅱ卷)高考数学理科试卷及答案解析
猜您在找
-

2022-2023学年江西省南昌市西湖区名校联盟七年级(下册)期中数学试卷word
-

2022-2023学年江西省南昌市南昌县七年级(下册)期中数学试卷word
-

人教版数学四年级上册期末复习卷word版
-

2022-2023学年江西省南昌市七年级(上册)期末数学试卷word版
-

2022-2023学年江西省赣州市寻乌县六年级(上)期末数学试卷+(参考答案解析word版)
-
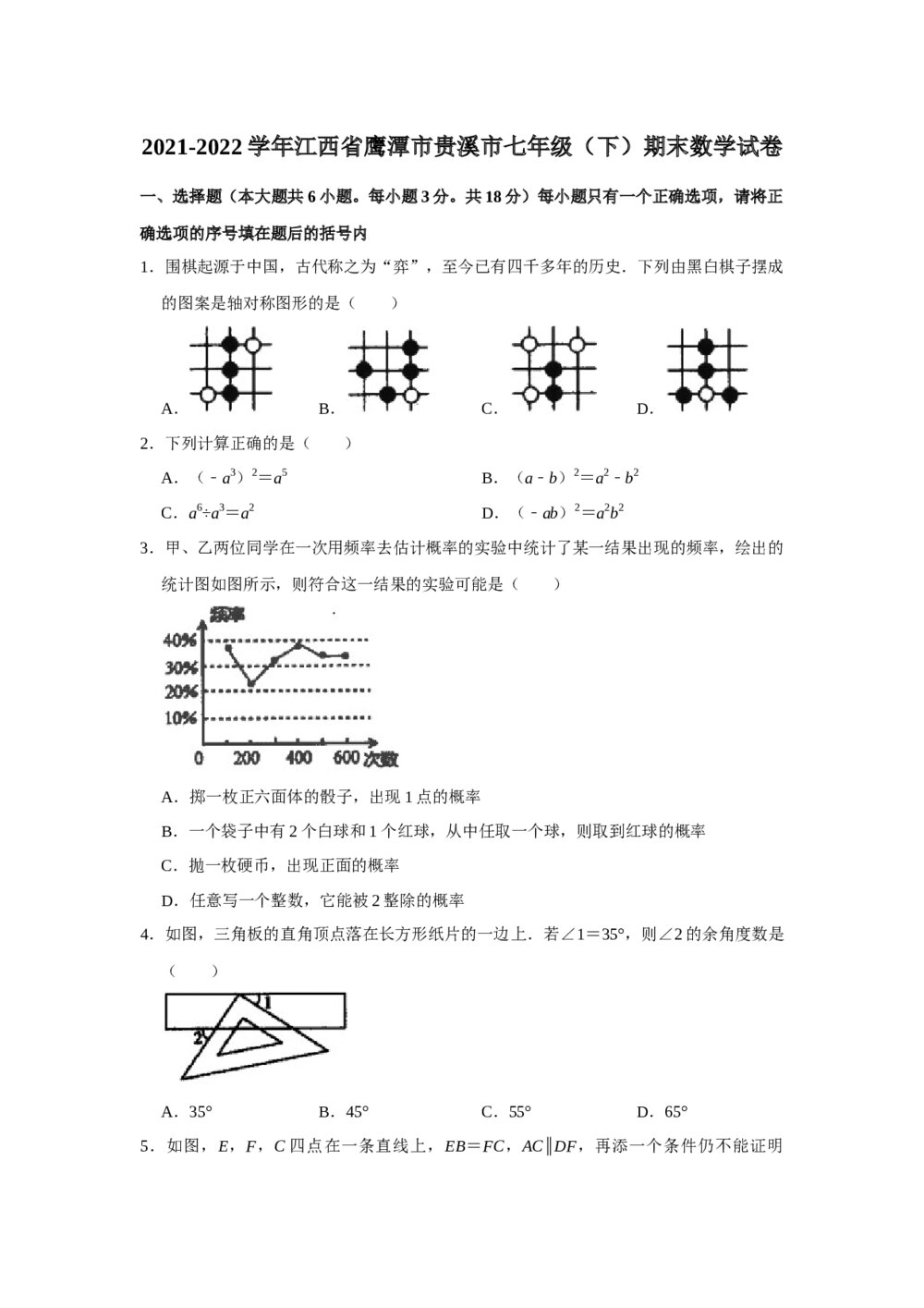
2021-2022学年江西省鹰潭市贵溪市七年级(下)期末数学试卷+(无答案Word版)
-

江西南昌东湖区邮政路小学2018学年四年级(下)数学期末检测试卷+答案解析版
-

2021-2022学年江西省新余市七年级(下)期末数学试卷+(答案解析word版)
-

2021-2022学年江西省宜春市袁州区宜阳学校六年级(上)期末数学试卷+(答案word版)
-

2021-2022学年江西省赣州区六年级(下)期末数学试卷+(答案word版)
-

2021-2022学年江西省抚州市南丰县六年级上学期期末数学试卷+(答案word版)
-

2020-2021学年江西省赣州市六年级(上)期末数学试卷+(答案word版)

 赣公网安备 36010802000481号
赣公网安备 36010802000481号